Liên hệ tuyển sinh
HIỆU QUẢ CỦA AZITHROMYCIN UỐNG SO VỚI GIẢ DƯỢC TRÊN CÁC TRIỆU CHỨNG COVID-19 Ở BỆNH NHÂN NGOẠI TRÚ VỚI NHIỄM SAR-COV-2- MỘT THỬ NGHIỆM LÂM SÀNG NGẪU NHIÊN
Nguồn:
CatherineE. Oldenburg, ScD,MPH1,2,3; BenjaminA. Pinsky, MD, PhD4,5,6; Jessica Brogdon, MPH,TM1; etalCindi Chen, MS1; Kevin Ruder, BS1; Lina Zhong, BS1; Fanice Nyatigo, BS1; CatherineA. Cook, MPH1; Armin Hinterwirth, PhD1; Elodi e Lebas, RN1; Travis Redd, MD, MPH1,2; Travis C. Porco, PhD, MPH1,2,3; Thomas M. Lietman, MD1,2,3; Benjamin F. Arnold, PhD, MPH1,2; Thuy Doan, MD, PhD1,2
Author Affiliations Article Information
JAMA. 2021;326(6):490-498. doi:10.1001/jama.2021.11517
CÁC ĐIỂM CHÍNH
Câu hỏi: Liệu một liều azithromycin uống duy nhất có dẫn đến mất triệu chứng vào ngày thứ 14 ở bệnh nhân nhiễm COVID-19 ngoại trú so với giả dược không?
Kết quả: Trong thử nghiệm ngẫu nhiên này gồm 263 người tham gia bị nhiễm SARS-CoV-2, điều trị bằng một liều uống duy nhất của azithromycin, 1,2 g dẫn đến kết quả được báo cáo là không có các triệu chứng COVID-19 ở ngày 14 với tỷ lệ 50% so với 50% dùng giả dược; điều này không có ý nghĩa thống kê.
Ý nghĩa: Trong số những bệnh nhân ngoại trú bị nhiễm SARS-CoV-2, điều trị bằng một liều azithromycin uống duy nhất so với giả dược không dẫn đến khả năng hết triệu chứng cao hơn vào ngày thứ 14.
TÓM TẮT
Tầm quan trọng: Azithromycin đã được giả thuyết là có hoạt tính chống lại SARS-CoV-2.
Mục tiêu: Để xác định xem liệu azithromycin đường uống ở bệnh nhân ngoại trú bị nhiễm SARS-CoV-2 có dẫn đến không có các triệu chứng COVID-19 vào ngày thứ 14 hay không.
Thiết kế và Người tham gia nghiên cứu: Thử nghiệm lâm sàng ngẫu nhiên của azithromycin so với giả dược phù hợp được tiến hành từ tháng 5 năm 2020 đến tháng 3 năm 2021. Bệnh nhân ngoại trú từ Hoa Kỳ được đăng ký từ xa thông qua các cuộc khảo sát dựa trên internet và được theo dõi trong 21 ngày. Những người tham gia đủ điều kiện có kết quả xét nghiệm chẩn đoán SARS-CoV-2 dương tính (PCR hoặc kháng nguyên) trong vòng 7 ngày trước khi đăng ký, từ 18 tuổi trở lên và không phải nhập viện tại thời điểm đăng ký. Trong số 604 người được sàng lọc, 297 người không đủ điều kiện, 44 người từ chối tham gia và 263 người đã đăng ký. Những người tham gia, điều tra viên và nhân viên nghiên cứu được che giấu để điều trị ngẫu nhiên.
Các can thiệp: Những người tham gia được chọn ngẫu nhiên theo kiểu 2: 1 với một liều azithromycin 1,2 g uống duy nhất (n = 171) hoặc giả dược phù hợp (n = 92).
Các kết quả chính và các biện pháp: Kết quả chính là không có các triệu chứng COVID-19 được báo cáo vào ngày thứ 14. Có 23 điểm kết thúc lâm sàng thứ cấp, bao gồm nhập viện do mọi nguyên nhân vào ngày 21.
Kết quả: Trong số 263 người tham gia được chọn ngẫu nhiên (tuổi trung bình, 43 tuổi; 174 (66%) phụ nữ; 57% người da trắng không phải gốc Tây Ban Nha và 29% người Latinx / gốc Tây Ban Nha), 76% đã hoàn thành thử nghiệm. Cuộc thử nghiệm đã bị chấm dứt bởi ủy ban giám sát dữ liệu và an toàn vì không có giá trị hữu ích sau khi phân tích tạm thời. Vào ngày 14, không có sự khác biệt đáng kể về tỷ lệ người tham gia không có triệu chứng (azithromycin: 50%; giả dược: 50%; chênh lệch tỷ lệ hiện mắc, 0%; KTC 95%, −14% đến 15%; P> 0.99). Trong số 23 điểm kết thúc lâm sàng thứ cấp được xác định trước, 18 điểm không có sự khác biệt đáng kể. Đến ngày 21, 5 người tham gia nhóm azithromycin phải nhập viện so với 0 người ở nhóm dùng giả dược (chênh lệch tỷ lệ hiện mắc, 4%; KTC 95%, −1% đến 9%; P = .16).
Kết luận và mức độ liên quan: Trong số những bệnh nhân ngoại trú bị nhiễm SARS-CoV-2, điều trị bằng một liều azithromycin duy nhất so với giả dược không dẫn đến khả năng hết triệu chứng cao hơn vào ngày thứ 14. Những phát hiện này không ủng hộ việc sử dụng azithromycin thường quy cho bệnh nhân SARS ngoại trú nhiễm Sar-CoV-2.
GIỚI THIỆU
Azithromycin là một kháng sinh azalide phổ rộng có đặc tính chống viêm và kháng vi-rút và đã được giả thuyết là có hoạt tính chống lại SARS-CoV-21. Tác dụng chống viêm của azithromycin có thể làm giảm mức cytokine có thể giúp ngăn ngừa sự tiến triển của tổn thương mô ở bệnh nhân nhiễm COVID-19 nặng, đặc biệt nếu được sử dụng sớm trong giai đoạn bệnh1. Nếu được phát hiện có hiệu quả, azithromycin không đắt, phổ biến rộng rãi và có tính an toàn tuyệt vời và sẽ là một ứng cử viên hấp dẫn để sử dụng ngoại trú. Ngoài ra, nếu thấy không có hiệu quả, nên hạn chế sử dụng nó để ngăn chặn việc lựa chọn kháng macrolide2.
Các thử nghiệm lâm sàng ngẫu nhiên trên bệnh nhân nhập viện và bệnh nhân ngoại trú với COVID-19 hiện không tìm thấy bằng chứng hỗ trợ việc sử dụng azithromycin để điều trị COVID-19 có hoặc không sử dụng hydroxychloroquine. Ở những bệnh nhân bị nhiễm SARS-CoV-2 đã được phòng thí nghiệm xác nhận có thể cung cấp bằng chứng chắc chắn hơn về hiệu quả của nó đối với COVID-19. Thử nghiệm lâm sàng ngẫu nhiên này trên bệnh nhân ngoại trú bị nhiễm SARS-CoV-2 được ghi nhận gần đây để đánh giá liệu một liều azithromycin uống duy nhất có hiệu quả để ngăn ngừa sự tiến triển của COVID-19 ở bệnh nhân ngoại trú hay không.
PHƯƠNG PHÁP NGHIÊN CỨU
Thiết kế nghiên cứu
Nghiên cứu Azithromycin cho thử nghiệm COVID-19, Điều tra Bệnh nhân Ngoại trú trên Toàn quốc (ACTION) là một thử nghiệm lâm sàng ngẫu nhiên 2: 1 đánh giá hiệu quả của một liều azithromycin 1,2 g uống duy nhất so với giả dược về các triệu chứng COVID-19 tự báo cáo ở bệnh nhân ngoại trú ở Mỹ. Những người tham gia được tuyển chọn từ ngày 22/5/2020 đến ngày 16/3/2021. Quá trình theo dõi hoàn tất vào ngày 31/3/2021. Nghiên cứu đã được xem xét và phê duyệt bởi các hội đồng đánh giá thể chế tại Đại học California, San Francisco (protocol 20-30504) và Đại học Stanford (protocol 56834) và được tiến hành theo đơn đăng ký Thuốc Mới Điều tra (Số 149526) từ Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA). Tất cả những người tham gia đã hoàn thành quy trình đồng ý bằng văn bản được thông báo bằng văn bản điện tử bằng tiếng Anh hoặc tiếng Tây Ban Nha. Để hoàn thành quy trình đồng ý được thông báo, nhân viên nghiên cứu đã xem xét nghiên cứu với những người tham gia, xem xét biểu mẫu đồng ý và trả lời bất kỳ câu hỏi nào. Nếu quan tâm, những người tham gia đã ký kỹ thuật số vào văn bản đồng ý đã được thông báo. Đề cương thử nghiệm và kế hoạch phân tích thống kê có trong Phụ lục 1.
Thiết lập và tuyển dụng nghiên cứu
Những người tham gia được tuyển chọn từ khắp Hoa Kỳ. Thử nghiệm đã được phổ biến thông qua các phương pháp truyền thống (ví dụ, tờ rơi ở các địa điểm xét nghiệm), thư gửi đến những bệnh nhân có kết quả xét nghiệm dương tính với SARS-CoV-2 tại Phòng thí nghiệm Vi rút Lâm sàng Stanford và phương tiện truyền thông xã hội. Những người tham gia tiềm năng đã hoàn thành một công cụ khảo sát trực tuyến để đánh giá tính đủ điều kiện của họ. Nhân viên nghiên cứu đã cố gắng liên hệ với từng người tham gia tiềm năng 3 lần qua điện thoại và một lần qua email nếu không thể liên lạc với người tham gia qua điện thoại. Nếu không liên lạc được với người tham gia tiềm năng hoặc không còn ở trong khoảng thời gian đủ điều kiện của họ kể từ ngày làm xét nghiệm SARS-CoV-2, họ được tính là “đủ điều kiện nhưng không đăng ký”. Nếu một người tham gia đã được liên hệ thành công, họ sẽ được cung cấp thông tin chi tiết về nghiên cứu và gửi bản sao điện tử của tài liệu đồng ý đã thông báo qua email. Những người tham gia không thể hoàn thành sự đồng ý được thông báo bằng điện tử đã được gửi một bản sao giấy của văn bản đồng ý qua đường bưu điện. Những người tham gia đã điền vào một cuộc khảo sát cơ bản trực tuyến và được gửi một bộ tài liệu nghiên cứu qua đường bưu điện, bao gồm thuốc nghiên cứu và hướng dẫn. Tất cả các tài liệu đều có sẵn bằng tiếng Anh và tiếng Tây Ban Nha. Chủng tộc và dân tộc do những người tham gia tự báo cáo dựa trên các danh mục cố định với tùy chọn báo cáo chủng tộc hoặc dân tộc “khác” để tuân thủ các hướng dẫn của Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ.
Đủ tiêu chuẩn nghiên cứu
Những người tham gia đủ điều kiện tham gia thử nghiệm nếu họ có kết quả xét nghiệm SARS-CoV-2 dương tính được ghi nhận (PCR hoặc kháng nguyên) trong vòng 7 ngày trước khi đăng ký. Nếu những người tham gia có nhiều xét nghiệm, ngày xét nghiệm dương tính đầu tiên được coi là ngày mà họ có kết quả dương tính. Những người tham gia đã tải lên bằng chứng về kết quả xét nghiệm dương tính với SARS-CoV-2 trong quá trình sàng lọc hoặc gửi kết quả qua email trực tiếp cho nhân viên nghiên cứu. Những người tham gia bị loại trừ nếu họ dưới 18 tuổi, bị dị ứng macrolide, đang đồng thời dùng hydroxychloroquine nếu họ trên 55 tuổi (để giảm nguy cơ kéo dài khoảng QT), đang dùng đồng thời nelfinavir hoặc warfarin, hiện đang mang thai (tự báo cáo), hoặc không thể nhận thuốc nghiên cứu qua đường bưu điện hoặc để hoàn thành bảng câu hỏi trực tuyến. Những người tham gia không được yêu cầu phải có triệu chứng để đủ điều kiện tham gia thử nghiệm.
Sự ngẫu nhiên
Những người tham gia được chọn ngẫu nhiên theo tỷ lệ 2: 1 với azithromycin hoặc giả dược phù hợp. Việc ngẫu nhiên không bị giới hạn (không chặn hoặc phân tầng) và trình tự được tạo bởi nhóm dữ liệu chưa được che giấu của nghiên cứu bằng cách sử dụng trình tạo số giả ngẫu nhiên do máy tính tạo ra trong R (R Foundation). Tỷ lệ phân bổ 2: 1 đã được chọn để tăng xác suất những người tham gia nhận được thuốc nghiên cứu tích cực mà không ảnh hưởng đến sức mạnh thống kê. Tỷ lệ phân bổ 2: 1 dẫn đến mức tăng tổng thể khoảng 10% so với tỷ lệ phân bổ 1: 1.
Can thiệp và làm mù
Để tạo điều kiện thuận lợi cho việc làm mù và làm mù phân bổ, các chữ cái đã được chỉ định ngẫu nhiên (ví dụ: A, B, C; tổng cộng 6 chữ cái) cho mỗi điều trị nghiên cứu (azithromycin hoặc giả dược). Ghi nhãn chai thuốc nghiên cứu giống hệt với ngoại trừ của thư điều trị để cho phép làm mù của các điều tra viên, nhân viên nghiên cứu và những người tham gia. Những người tham gia được chỉ định ngẫu nhiên để nhận 1 trong 6 lá thư điều trị và được gửi một lọ thuốc có nhãn điều trị đó. Chỉ nhóm dữ liệu không đươc tiết lộ của nghiên cứu mới biết được những chữ cái điều trị nào tương ứng với azithromycin và giả dược. Sau khi phân loại ngẫu nhiên, những người tham gia được gửi một liều duy nhất 1,2 g hỗn dịch azithromycin hoặc giả dược phù hợp (Pfizer Inc) qua đường bưu điện qua đêm. Giả dược được bào chế đặc biệt để phù hợp với azithromycin. Việc phân bổ được che giấu bằng cách không tiết lộ bức thư được giao ngẫu nhiên cho người tham gia cho đến khi hoàn tất việc ghi danh và đánh giá cơ bản.
Trong trường hợp bác sĩ điều trị của người tham gia nghiên cứu cho rằng cần thiết cho sự an toàn của người tham gia để biết họ nhận azithromycin hay giả dược, một thành viên không giấu mặt của nhóm nghiên cứu đã liên hệ trực tiếp với bác sĩ điều trị để tiết lộ thông tin này. Thông tin phân bổ điều trị chỉ được tiết lộ khi có yêu cầu của bác sĩ điều trị.
Kết cục
Tất cả các điểm kết thúc lâm sàng chính và phụ đã xác định trước đều được báo cáo ở đây (xem Phụ lục 1 để biết danh sách đầy đủ các điểm kết thúc chính và phụ được xác định trước). Điểm kết thúc chính xác định trước là tự báo cáo không có các triệu chứng COVID-19 vào ngày 14. Điểm cuối phụ được xác định trước bao gồm các tác dụng phụ ở ngày thứ 3, nhập viện và/hoặc tử vong vào ngày 21, khoa cấp cứu và/hoặc sử dụng dịch vụ chăm sóc khẩn cấp vào ngày 21, các thành viên trong gia đình đã được chẩn đoán hoặc phát triển các triệu chứng của COVID-19 vào ngày 21 và các triệu chứng COVID-19 được bệnh nhân báo cáo vào ngày 21 (bao gồm sốt, ho, tiêu chảy, đau bụng, thiếu máu, viêm kết mạc, đau họng, khó thở, đau cơ, mệt mỏi, chóng mặt và danh mục “khác” kết thúc mở). Điểm cuối của phòng thí nghiệm sẽ được báo cáo trong một bài báo riêng.
Đánh giá kết cục
Những người tham gia đã hoàn thành khảo sát trực tuyến vào các ngày 3, 7, 14 và 21 sau khi ghi danh để đánh giá kết quả. Vào ngày thứ 3, những người tham gia được hỏi liệu họ có bị nôn, buồn nôn, tiêu chảy, phát ban hoặc đau bụng hay không kể từ khi họ uống thuốc nghiên cứu để đánh giá các tác dụng phụ có thể xảy ra của thuốc nghiên cứu. Những người tham gia được hỏi về các triệu chứng tại mỗi thời điểm. Những người tham gia được hỏi liệu họ đã ở trong bệnh viện (được định nghĩa là trong khoa cấp cứu hoặc nhập viện trong hơn 24 giờ), nếu họ đã đến phòng cấp cứu hoặc trung tâm chăm sóc khẩn cấp, và nếu bất kỳ thành viên nào trong gia đình đã được chẩn đoán hoặc phát triển các triệu chứng của COVID-19 kể từ cuộc khảo sát cuối cùng của họ.
Các thay đổi Protocol
Kết quả chính ban đầu của thử nghiệm là nhập viện. Trước phân tích tạm thời đầu tiên, tỷ lệ người tham gia phải nhập viện về cơ bản thấp hơn 10% so với giả định trong giai đoạn thiết kế thử nghiệm ban đầu (Phần bổ sung 1). Do nguy cơ nhập viện thấp hơn và nhập viện chậm hơn dự kiến, các nhà điều tra chính đã đề xuất với ủy ban giám sát dữ liệu và an toàn (DSMC) vào ngày 15/10/2020, rằng kết quả chính được thay đổi thành không có các triệu chứng tự báo cáo sau 14 ngày nghiên cứu, không tiết lộ việc phân bổ điều trị hoặc thực hiện bất kỳ phân tích dữ liệu nào. DSMC đã chấp thuận thay đổi này trong cùng ngày. Nhà thống kê của nghiên cứu đã xác định lại cỡ mẫu cho kết quả chính mới (được mô tả trong phần Cỡ mẫu) và một lịch trình giám sát tạm thời mới được đề xuất bao gồm một phân tích tạm thời duy nhất khi một nửa mục tiêu cỡ mẫu mới đã được đăng ký và đạt được sau 14 ngày (được mô tả trong phần Phân tích Tạm thời). Các thay đổi đã được thực hiện trong kế hoạch phân tích thống kê, trong sổ tay hướng dẫn hoạt động và thủ tục, và trên ClinicalTrials.gov vào ngày 15/12/2020, trước khi phân tích tạm thời hoặc tiết lộ việc phân bổ điều trị.
Giám sát thử nghiệm
DSMC, bao gồm các chuyên gia về thống kê sinh học, thiết kế thử nghiệm, dịch tễ học và bệnh truyền nhiễm, giám sát thử nghiệm. DSMC đã họp 3 lần trong suốt quá trình thử nghiệm để xem xét và phê duyệt thiết kế nghiên cứu trước khi bắt đầu đăng ký, để xem xét các thay đổi được đề xuất trong điểm kết thúc chính và xem xét kết quả phân tích tạm thời. Đề cương nghiên cứu quy định rằng các tác dụng phụ nghiêm trọng phải được báo cáo cho người giám sát y tế của nghiên cứu, người này sau đó sẽ xác định xem chúng có liên quan đến việc tham gia nghiên cứu hay không. Bất kỳ sự kiện bất lợi nghiêm trọng nào được xác định là có thể liên quan đến việc tham gia nghiên cứu phải được báo cáo cho DSMC trong thời gian thực.
Cỡ mẫu
Ước tính cỡ mẫu ban đầu dựa trên kết quả chính ban đầu, nhập viện vào ngày 14 (Phụ lục 1). Mục tiêu cỡ mẫu đã được sửa đổi sau khi thay đổi điểm kết thúc chính thành không có các triệu chứng tự báo cáo ở ngày thứ 14. Giả sử 50% người tham gia sẽ không còn triệu chứng vào ngày 14, 20% mất thời gian theo dõi và α = .05, bao gồm 455 người tham gia sẽ cung cấp khoảng 80% sức mạnh để phát hiện sự gia tăng tỷ lệ người tham gia không có triệu chứng từ 50% lên 65% ở ngày thứ 14. Tại thời điểm thử nghiệm được thiết kế, có rất ít bằng chứng để hướng dẫn giả định về kích thước mẫu. Sự khác biệt 15% được chọn bởi vì nó được đánh giá là sự khác biệt có ý nghĩa lâm sàng, kích thước mẫu sẽ khả thi để tuyển dụng và sự khác biệt này phù hợp với sự cải thiện lâm sàng ở 14 ngày trong một thử nghiệm ban đầu của lopinavir-ritonavir và với các giả định khác các thử nghiệm đang diễn ra của azithromycin đối với COVID-197,8.
Phân tích tạm thời
Một phân tích hiệu quả tạm thời duy nhất sau khi 50% dân số mục tiêu đã đăng ký và đã đạt đến điểm kết thúc ngày 14 của họ được xác định trước (P = 0,001) bằng cách sử dụng phương pháp tiếp cận Lan-DeMets α với ranh giới O’Brien-Fleming
Phân tích thống kê
Trong trường hợp thử nghiệm bị dừng vì bất kỳ lý do gì, phân tích cuối cùng được chỉ định trước sẽ bao gồm tất cả các kết quả giữa những người tham gia đã đăng ký vào thời điểm thử nghiệm bị dừng. Những người tham gia được phân tích theo nhóm ngẫu nhiên của họ và tất cả những người tham gia có dữ liệu đầy đủ ở ngày 14 đều được đưa vào phân tích sơ cấp. Các phương pháp xử lý dữ liệu bị thiếu trong phân tích độ nhạy được mô tả dưới đây. Phân tích ban đầu ước tính sự khác biệt về tỷ lệ hiện mắc so sánh tỷ lệ bệnh nhân không có triệu chứng sau 14 ngày ở nhóm azithromycin và nhóm giả dược. Tỷ lệ phổ biến và khoảng tin cậy tương ứng 95% được ước tính bằng cách sử dụng sơ đồ khởi động không tham số. Giá trị P cho sự khác biệt giữa các nhóm được tính toán bằng cách sử dụng thử nghiệm hoán vị với sự khác biệt phổ biến giữa các nhóm làm thống kê thử nghiệm và 10000 lần lặp. Đối với các điểm cuối phụ của việc nhập viện, sử dụng phòng cấp cứu, sự cố COVID-19 giữa các thành viên khác trong gia đình và các triệu chứng COVID-19 cụ thể, sự khác biệt về tỷ lệ hiện mắc giữa các nhóm và khoảng tin cậy 95% cho sự khác biệt được ước tính. Giá trị P được ước tính cho sự khác biệt giữa các nhóm với kết quả chính. Tỷ lệ người tham gia trải qua mỗi tác dụng phụ được tính toán theo nhóm điều trị.
Một loạt phân tích phân nhóm cho điểm kết thúc chính đã được xác định trước, bao gồm theo độ tuổi (> 60 so với ≤ 60 tuổi), sự hiện diện của các triệu chứng COVID-19 tự báo cáo so với không có triệu chứng, và nguy cơ cao so với nguy cơ thấp, với cao nguy cơ được xác định là từ 60 tuổi trở lên và được báo cáo có tăng huyết áp, bệnh tim mạch, đái tháo đường, hoặc bệnh phổi tắc nghẽn hoặc hạn chế (Phụ lục 1). Sự hiện diện của tương tác trên thang cộng được thử nghiệm để sử dụng thuật ngữ tương tác giữa nhóm điều trị và từng công cụ điều chỉnh hiệu ứng trong các mô hình nhị thức tuyến tính. Bởi vì tất cả các phân tích đã được xác định trước, không có điều chỉnh nào cho nhiều so sánh được thực hiện. Tất cả các thử nghiệm đều có 2 mặt và α < 0.05 được coi là có ý nghĩa thống kê. Do có khả năng mắc lỗi loại I do nhiều lần so sánh, các kết quả phân tích các điểm cuối phụ nên được hiểu là khám phá.
Một phân tích xác định trước để tính đến các kết quả bị thiếu bằng cách sử dụng trọng số xác suất nghịch đảo đã được hoàn thành như một phép kiểm tra độ chắc chắn, giả định rằng các kết quả bị thiếu một cách ngẫu nhiên (Phần bổ sung 1)9. Để kiểm tra độ chắc chắn bổ sung, giả sử rằng các kết quả bị thiếu không phải ngẫu nhiên, phương pháp tiếp cận mô hình hỗn hợp mẫu đã được sử dụng mô hình hóa trường hợp không có triệu chứng ở ngày 14 với mô hình xác suất tuyến tính dưới dạng hàm hiệp biến được liệt kê cho công cụ ước lượng xác suất nghịch đảo. Kết quả bị thiếu được đưa ra bằng cách sử dụng mô hình phù hợp để dự đoán, thêm một tham số dịch chuyển khác nhau trên một loạt giá trị. Tất cả các phân tích được thực hiện trong phiên bản R 4.0.2 (R Foundation).
KẾT QUẢ
Tổng cộng 263 người tham gia đã được ghi danh, trong đó 171 người được chọn ngẫu nhiên với azithromycin và 92 người dùng giả dược, với 76% hoàn thành nghiên cứu ngày 14 (77% ở nhóm azithromycin và 76% ở nhóm giả dược) (Hình; eTable 1 trong Bổ sung 2). Tỷ lệ phần trăm và sự phân bố các đặc điểm cơ bản giữa những người tham gia hoàn thành thử nghiệm và những người đã dùng và không báo cáo việc dùng thuốc nghiên cứu là tương tự giữa các nhóm (Bảng điện tử 2-5 trong Phần bổ sung 2). Thời gian trung bình từ khi có kết quả xét nghiệm dương tính đến khi tham gia vào nghiên cứu là 3 ngày (azithromycin: 3 ngày; giả dược: 2 ngày) (Bảng 1). Độ tuổi trung bình của dân số nghiên cứu là 43 tuổi và 66% là nữ. Các triệu chứng phổ biến nhất được báo cáo lúc ban đầu bao gồm ho (azithromycin: 65%; giả dược: 66%), mệt mỏi (azithromycin: 63%; giả dược: 60%) và sốt (azithromycin: 51%; giả dược: 44%) (Bảng 1). Hầu hết những người tham gia báo cáo có nhiều triệu chứng (azithromycin: 89%; giả dược: 89%). Thông tin phân bổ điều trị đã được cung cấp cho các bác sĩ điều trị của 4 người tham gia.
Dân số phân tích tạm thời đã đạt được vào ngày 3/2/2021. Khi xem xét phân tích tạm thời được chỉ định trước, DSMC đã yêu cầu đánh giá quyền lực có điều kiện để đưa ra khuyến nghị về việc tiếp tục thử nghiệm10. Phân tích này mang lại quyền lực có điều kiện là 17% với giả định là dữ liệu cho Phần còn lại của thử nghiệm phù hợp với tỷ lệ bệnh nhân không có triệu chứng tự báo cáo ở nhóm azithromycin tăng 15 điểm phần trăm so với nhóm dùng giả dược. Do quyền lực có điều kiện thấp và lưu ý rằng việc tuyển dụng mất nhiều thời gian hơn so với dự đoán ban đầu, DSMC đã khuyến nghị dừng nghiên cứu vào ngày 16/3/2021.

Figure. Flow of Participants in a Trial of Azithromycin for Treatment of SARS-CoV-2 Infection in Outpatients
Kết cục chính
Tỷ lệ người tham gia báo cáo không có triệu chứng ở lần khảo sát ngày 14 không có sự khác biệt có ý nghĩa giữa các nhóm (50% số người tham gia trong mỗi nhóm) (Bảng 2). Điều này tương ứng với sự khác biệt về tỷ lệ hiện mắc là 0% (KTC 95%, -14% đến 15%; P> 0.99) và tỷ lệ hiện mắc là 1.01 (KTC 95%, 0.76-1.39; P> 0.99).
Năm người tham gia được coi là có nguy cơ cao theo định nghĩa đã xác định trước, loại trừ phân tích phân nhóm theo phân tầng rủi ro. Giữa các cá nhân từ 60 tuổi trở xuống, sự khác biệt về tỷ lệ hiện mắc là 0% (95% CI, -15% - 16%), và giữa những người trên 60 tuổi, sự khác biệt về tỷ lệ là 0% (95% CI, -46% - 46%), không có sự khác biệt đáng kể về ước tính giữa các nhóm (P> .99 đối với tương tác) (Bảng 2). Tương tự, không có sự khác biệt đáng kể giữa những người không có triệu chứng (tỷ lệ chênh lệch hiện mắc, 15%; KTC 95%, -46% - 76%) so với những người tham gia có triệu chứng (chênh lệch tỷ lệ hiện mắc, -1%; KTC 95%, -17% - 15%; P = .52 cho tương tác) (Bảng 2). Phân tích độ nhạy giả định dữ liệu bị thiếu ngẫu nhiên bằng cách sử dụng trọng số xác suất nghịch đảo (tỷ lệ chênh lệch hiện mắc, 0%; KTC 95%, -15% - 15%) và dữ liệu bị thiếu không ngẫu nhiên (giả sử tỷ lệ không có triệu chứng giảm 4 lần tại ngày 14 trong số những dữ liệu bị thiếu đó, có điều kiện dựa trên tất cả các hiệp biến đo được khác, tỷ lệ chênh lệch hiện mắc, 1%; KTC 95%, -14% - 15%) phù hợp với kết quả chính (eTable 6 trong Phần bổ sung 2). Các giả định thay đổi đối với sự thiếu sót không phải trong các phân tích ngẫu nhiên đều phù hợp với kết quả chính (eTable 6).
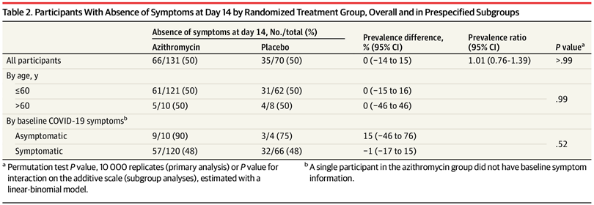
Table 2. Participants With Absence of Symptoms at Day 14 by Randomized Treatment Group, Overall and in Prespecified Subgroups
Kết cục thứ phát
Đến ngày thứ 3, nhiều người tham gia báo cáo các tác dụng phụ trên đường tiêu hóa ở nhóm azithromycin so với giả dược, bao gồm tiêu chảy (azithromycin: 41%; giả dược: 17%), đau bụng (azithromycin: 17%; giả dược: 1%) và buồn nôn (azithromycin: 22%; giả dược: 10%) (Bảng 3). Không có sự khác biệt đáng kể về các triệu chứng COVID-19 tự báo cáo cụ thể được báo cáo ở ngày thứ 14 (Bảng 4). Không có tác dụng phụ nghiêm trọng nào được báo cáo, và không có trường hợp tử vong nào trong cả hai nhóm nghiên cứu. Trong số những người tham gia được theo dõi đến ngày 21, 5 người báo cáo đã nhập viện, tất cả đều thuộc nhóm azithromycin (Bảng 4). Các lý do nhập viện bao gồm khó thở (n = 2), viêm phổi (n = 1), độ bão hòa oxy thấp (n = 1) và đau bụng (n = 1). Đến ngày thứ 21, các lần khám cấp cứu / chăm sóc khẩn cấp ở nhóm azithromycin cao hơn đáng kể so với nhóm giả dược (azithromycin: 14%; giả dược: 3%; khác biệt, 12%; KTC 95%, 3% -20%; P = .01) (Bảng 4). Không có sự khác biệt đáng kể trong 18 kết quả phụ khác (Bảng 4).
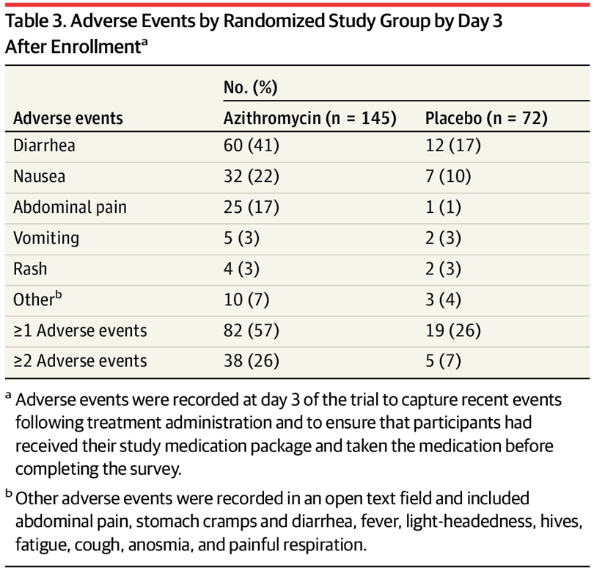
Table 3. Adverse Events by Randomized Study Group by Day 3 After Enrollmenta
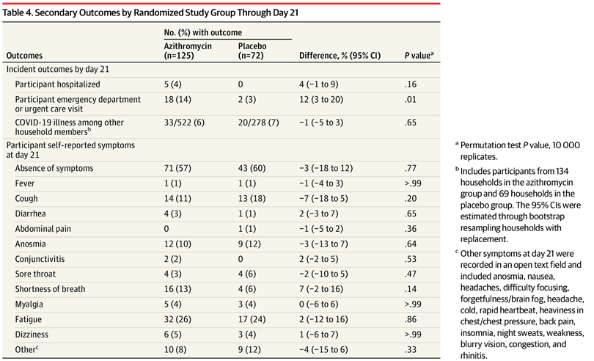
Table 4. Secondary Outcomes by Randomized Study Group Through Day 21
BÀN LUẬN
Trong thử nghiệm lâm sàng ngẫu nhiên này về azithromycin uống liều duy nhất cho bệnh nhân ngoại trú nhiễm COVID-19, không có sự khác biệt đáng kể về sự vắng mặt của các triệu chứng tự báo cáo 14 ngày sau khi tham gia nghiên cứu giữa những người tham gia ngẫu nhiên với azithromycin so với giả dược. Những kết quả này được xây dựng dựa trên các thử nghiệm lâm sàng ngẫu nhiên trước đây về azithromycin đối với COVID-19 ở cả bệnh nhân ngoại trú và nội trú, không có kết quả nào trong số đó tìm thấy lợi ích của azithromycin trong việc điều trị COVID-193-6,11. Ở bệnh nhân nhập viện, các thử nghiệm của azithromycin có hoặc không có hydroxychloroquine không tìm thấy tác dụng của azithromycin trên kết quả lâm sàng hoặc tử vong, không có tín hiệu an toàn rõ ràng4,5,11. Ở những bệnh nhân ngoại trú và những người nghi ngờ mắc bệnh COVID-19, azithromycin không ngăn được sự tiến triển của việc nhập viện hoặc cải thiện thời gian thanh thải virus SARS-CoV-2 trong gạc mũi3,6. Thử nghiệm hiện tại bổ sung thêm bằng chứng chống lại lợi ích lâm sàng của azithromycin đối với COVID-19.
Hầu hết những người tham gia tham gia thử nghiệm này đều có triệu chứng ở thời điểm ban đầu, và sự phân bố các triệu chứng phản ánh các bối cảnh khác. Việc đăng ký không bị hạn chế dựa trên các triệu chứng, mức độ nghiêm trọng của bệnh, hoặc nguy cơ tiến triển thành bệnh nặng để đánh giá xem azithromycin có hiệu quả rất sớm trong COVID-19 trước khi nó tiến triển hay không. Những kết quả này không thể ngoại suy cho những bệnh nhân mắc bệnh nặng hơn hoặc những bệnh nhân có nguy cơ tiến triển cao hơn.
Các phân tích thứ cấp thăm dò đánh giá các kết quả lâm sàng như nhập viện và sử dụng tại khoa cấp cứu và nên được hiểu là tạo ra giả thuyết. Các tác dụng ngoại ý nhẹ trên đường tiêu hóa sau khi dùng azithromycin được xác định rõ ràng14-16. Những người tham gia dùng azithromycin báo cáo nhiều tác dụng phụ trên đường tiêu hóa hơn sau khi điều trị 3 ngày so với giả dược. Tất cả các trường hợp nhập viện xảy ra ở nhóm azithromycin, và có nhiều trường hợp sử dụng tại khoa cấp cứu hơn ở nhóm azithromycin so với giả dược. Hầu hết các trường hợp nhập viện là do các vấn đề về hô hấp, mặc dù có 1 người tham gia báo cáo nhập viện vì đau bụng dữ dội. Nghiên cứu bổ sung là cần thiết để xác nhận những phát hiện này.
Việc lạm dụng kháng sinh quá mức trong đại dịch COVID-19 có thể dẫn đến việc tăng cường đề kháng kháng sinh17,18. Những người tham gia báo cáo việc sử dụng macrolide gần đây không bị loại trừ; 12.5% người tham gia báo cáo rằng họ đã sử dụng macrolide trong vòng 30 ngày kể từ ngày tham gia nghiên cứu. Điều trị bằng kháng sinh được biết đến là phương pháp chọn lọc để kháng thuốc.
HẠN CHẾ NGHIÊN CỨU
Kết quả nghiên cứu này có một số hạn chế. Đầu tiên, mặc dù thử nghiệm ban đầu được thiết kế để đánh giá việc ngăn ngừa nhập viện, do tỷ lệ biến cố thấp hơn dự kiến, kết quả chính được thay đổi thành không có triệu chứng vào ngày 14 trước khi phân tích tạm thời đầu tiên. Nghiên cứu này không đủ khả năng cho các điểm kết thúc nhập viện. Thứ hai, một tỷ lệ đáng kể những người tham gia báo cáo không dùng thuốc nghiên cứu được phân bổ của họ hoặc thiếu dữ liệu về tuân thủ. Không tuân thủ loại thuốc nghiên cứu được phân bổ có thể có kết quả sai lệch về phía vô hiệu. Thứ ba, tổn thất để theo dõi cao hơn so với kế hoạch. Nghiên cứu được thực hiện từ xa mà không có bất kỳ sự tiếp xúc nào của bệnh nhân để giảm nguy cơ lây truyền, điều này có thể tạo điều kiện thuận lợi cho việc theo dõi. Email, điện thoại và thông tin thân nhân đã được thu thập từ tất cả những người tham gia. Nhiều lời nhắc đã được gửi để hoàn thành các cuộc khảo sát nhằm giảm thiểu mất mẫu khi theo dõi. Các đặc điểm cơ bản đối với những đặc điểm được giữ lại và không được giữ lại sau 14 ngày là tương tự nhau, và các phân tích độ nhạy tính đến các kết quả bị thiếu không thay đổi bất kỳ kết luận nào của nghiên cứu. Nếu những người tham gia đã nhập viện hoặc mất khả năng lao động không được theo dõi, việc nhập viện và các kết quả xấu khác có thể bị đánh giá thấp. Thứ tư, thời gian từ khi nhận được kết quả xét nghiệm dương tính đến khi tham gia vào nghiên cứu dài hơn trung bình 1 ngày ở những người tham gia được ngẫu nhiên dùng azithromycin so với giả dược. Khoảng thời gian dài hơn giữa kết quả xét nghiệm dương tính và ghi danh có thể có nghĩa là những người tham gia đó đã tiến xa hơn trong quá trình bệnh của họ và ít có khả năng mắc các triệu chứng dai dẳng hơn. Thứ năm, những người tham gia phải có khả năng hoàn thành bảng câu hỏi trực tuyến và nhận tài liệu nghiên cứu tại một địa điểm thực tế để tham gia thử nghiệm, có thể được lựa chọn cho nhóm dân số trẻ hơn và có nguy cơ thấp hơn, hạn chế khả năng tổng quát hóa đối với những người có nguy cơ tăng kết quả kém. Tuy nhiên, do azithromycin được kê đơn thường quy cho bệnh nhân mắc COVID-19 ở các phân nhóm nguy cơ thấp hơn, nên việc đưa vào rộng rãi có thể cải thiện khả năng tổng quát để quản lý bệnh nhân ngoại trú có nguy cơ thấp hơn.
KẾT LUẬN
Trong số những bệnh nhân ngoại trú bị nhiễm SARS-CoV-2, điều trị bằng một liều azithromycin duy nhất không dẫn đến khả năng hết triệu chứng cao hơn vào ngày thứ 14 so với giả dược. Những phát hiện này không ủng hộ việc sử dụng azithromycin thường quy cho bệnh nhân ngoại trú nhiễm SARS-CoV- 2.
Corresponding Author: Catherine E. Oldenburg, ScD, MPH, Francis I. Proctor Foundation, University of California, San Francisco, 490 Illinois St, Floor 2, San Francisco, CA 94143 (catherine.oldenburg@ucsf.edu).
Accepted for Publication: June 25, 2021.
Published Online: July 16, 2021. doi:10.1001/jama.2021.11517
Author Contributions: Drs Oldenburg and Arnold had full access to all of the data in the study and take responsibility for the integrity of the data and the accuracy of the data analysis.
TÀI LIỆU THAM KHẢO
1. Oliver ME, Hinks TSC. Azithromycin in viral infections. Rev Med Virol. 2021;31(2):e2163. doi:10.1002/rmv.2163PubMedGoogle Scholar
2. O’Brien KS, Emerson P, Hooper PJ, et al. Antimicrobial resistance following mass azithromycin distribution for trachoma: a systematic review. Lancet Infect Dis. 2019;19(1):e14-e25.doi:10.1016/S1473-3099(18)30444-4PubMedGoogle ScholarCrossref
3. PRINCIPLE Trial Collaborative Group. Azithromycin for community treatment of suspected COVID-19 in people at increased risk of an adverse clinical course in the UK (PRINCIPLE): a randomised, controlled, open-label, adaptive platform trial. Lancet. 2021;397(10279):1063-1074.doi:10.1016/S0140-6736(21)00461-XPubMedGoogle ScholarCrossref
4. Cavalcanti AB, Zampieri FG, Rosa RG, et al; Coalition Covid-19 Brazil I Investigators. Hydroxychloroquine with or without azithromycin in mild-to-moderate Covid-19. N Engl J Med. 2020;383(21):2041-2052. doi:10.1056/NEJMoa2019014PubMedGoogle ScholarCrossref
5. RECOVERY Collaborative Group. Azithromycin in the treatment of patients admitted to the hospital with severe COVID-19: the COALITION II randomised clinical trial. Lancet. 2021;397(10274):605-612. doi:10.1016/S0140-6736(21)00149-5PubMedGoogle ScholarCrossref
6. Johnston C, Brown ER, Stewart J, et al; COVID-19 Early Treatment Study Team. Hydroxychloroquine with or without azithromycin for treatment of early SARS-CoV-2 infection among high-risk outpatient adults: a randomized clinical trial. EClinicalMedicine. 2021;33:100773. doi:10.1016/j.eclinm.2021.100773PubMedGoogle Scholar
7. Cao B, Wang Y, Wen D, et al. A trial of lopinavir-ritonavir in adults hospitalized with severe Covid-19. N Engl J Med. 2020;382(19):1787-1799. doi:10.1056/NEJMoa2001282PubMedGoogle ScholarCrossref
8. Gyselinck I, Liesenborghs L, Landeloos E, et al; DAWn-Azithro Consortium. Direct antivirals working against the novel coronavirus: azithromycin (DAWn-AZITHRO), a randomized, multicenter, open-label, adaptive, proof-of-concept clinical trial of new antivirals working against SARS-CoV-2—azithromycin trial. Trials. 2021;22(1):126. doi:10.1186/s13063-021-05033-xPubMedGoogle ScholarCrossref
9. Little RJ, D’Agostino R, Cohen ML, et al. The prevention and treatment of missing data in clinical trials. N Engl J Med. 2012;367(14):1355-1360. doi:10.1056/NEJMsr1203730PubMedGoogle ScholarCrossref
10. Lachin JM. A review of methods for futility stopping based on conditional power. Stat Med. 2005;24(18):2747-2764. doi:10.1002/sim.2151PubMedGoogle ScholarCrossref
11. RECOVERY Collaborative Group. Azithromycin in patients admitted to hospital with COVID-19 (RECOVERY): a randomised, controlled, open-label, platform trial. Lancet. 2021;397(10274):605-612. doi:10.1016/S0140-6736(21)00149-5PubMedGoogle ScholarCrossref
12. Spinato G, Fabbris C, Polesel J, et al. Alterations in smell or taste in mildly symptomatic outpatients with SARS-CoV-2 infection. JAMA. 2020;323(20):2089-2090. doi:10.1001/jama.2020.6771
ArticlePubMedGoogle ScholarCrossref
13. Nehme M, Braillard O, Alcoba G, et al; COVICARE Team. COVID-19 symptoms: longitudinal evolution and persistence in outpatient settings. Ann Intern Med. 2021;174(5):723-725. doi:10.7326/M20-5926PubMedGoogle ScholarCrossref
14. Sié A, Dah C, Bountogo M, et al; Gamin Study Group. Adverse events and clinic visits following a single dose of oral azithromycin among preschool children: a randomized placebo-controlled trial. Am J Trop Med Hyg. 2020;104(3):1137-1141. doi:10.4269/ajtmh.20-1002PubMedGoogle Scholar
15. Ayele B, Gebre T, House JI, et al. Adverse events after mass azithromycin treatments for trachoma in Ethiopia. Am J Trop Med Hyg. 2011;85(2):291-294. doi:10.4269/ajtmh.2011.11-0056PubMedGoogle ScholarCrossref
16. Astale T, Sata E, Zerihun M, et al. Self-reported side effects following mass administration of azithromycin to eliminate trachoma in Amhara, Ethiopia: results from a region-wide population-based survey. Am J Trop Med Hyg. 2019;100(3):696-699. doi:10.4269/ajtmh.18-0781PubMedGoogle ScholarCrossref
17. Antimicrobial resistance in the age of COVID-19. Nat Microbiol. 2020;5(6):779. doi:10.1038/s41564-020-0739-4PubMedGoogle ScholarCrossref
18. Afshinnekoo E, Bhattacharya C, Burguete-García A, et al; MetaSUB Consortium. COVID-19 drug practices risk antimicrobial resistance evolution. Lancet Microbe. 2021;2(4):e135-e136. doi:10.1016/S2666-5247(21)00039-2PubMedGoogle ScholarCrossref
19. Lipsitch M, Samore MH. Antimicrobial use and antimicrobial resistance: a population perspective. Emerg Infect Dis. 2002;8(4):347-354. doi:10.3201/eid0804.010312PubMedGoogle ScholarCrossref
20. Doan T, Worden L, Hinterwirth A, et al. Macrolide and nonmacrolide resistance with mass azithromycin distribution. N Engl J Med. 2020;383(20):1941-1950. doi:10.1056/NEJMoa2002606PubMedGoogle ScholarCrossref
21. Oldenburg CE, Hinterwirth A, Sié A, et al. Gut resistome after oral antibiotics in preschool children in Burkina Faso: a randomized, controlled trial. Clin Infect Dis. 2020;70(3):525-527. doi:10.1093/cid/ciz455PubMedGoogle ScholarCrossref
Lược dịch: Bác sỹ CKII. Lê Xuân Túy*
* Bệnh viện Đa khoa Tâm Trí Đà Nẵng
Các tin khác
- Nghiên cứu mới: Kiến thức liên tục của bác sĩ nội khoa ảnh hưởng đến chất lượng điều trị ( 10:56 - 19/06/2025 )
- Đặc điểm lâm sàng và cận lâm sàng bệnh nhân hậu COVID-19 tại bệnh viện đa khoa Tâm Trí Sài Gòn: một nghiên cứu hồi cứu cắt ngang ( 14:59 - 10/05/2022 )
- MỐI LIÊN QUAN GIỮA MẸ BỊ NHIỄM SARS-CoV-2 VÀ DỰ HẬU TRÊN TRẺ SƠ SINH ( 13:33 - 31/05/2021 )
- TẦM SOÁT UNG THƯ ĐẠI TRỰC TRÀNG ( 09:00 - 20/05/2021 )
- KHÁNG THỂ ĐẶC HIỆU SARS-COV-2 TRONG SỮA MẸ SAU CHỦNG NGỪA VACCINE COVID-19 Ở NHỮNG PHỤ NỮ ĐANG CHO CON BÚ ( 08:27 - 20/05/2021 )
- Lợi ích của việc Tránh Chăm sóc Y tế Không cần thiết Trong Đại dịch COVID-19 ( 14:01 - 15/05/2021 )
- Rapid and sensitive diagnostic procedure for multiple detection of pandemic Coronaviridae family members SARS-CoV-2, SARS-CoV, MERS-CoV and HCoV: a translational research and cooperation between the Phan Chau Trinh University in Vietnam and Universit ( 15:42 - 29/06/2020 )
- Các nghiên cứu của PCTU tại hội nghị quốc tế ISSAR 2019 - Gyeongju, Hàn Quốc ( 16:17 - 04/11/2019 )
- Melioidosis in Vietnam: Recently Improved Recognition but still an Uncertain Disease Burden after Almost a Century of Reporting ( 13:29 - 27/04/2018 )
- Tác nhân vi sinh gây viêm phổi cộng đồng phải nhập viện ( 11:20 - 03/02/2018 )