Liên hệ tuyển sinh
Hợp tác Quốc tế
ĐÁP ỨNG KHÁNG THỂ SAU KHI TIÊM 2 LIỀU VACINE SARS-CoV-2 m RNA TRÊN NỀN BỆNH NHÂN GHÉP TẠNG
Bài dịch
ĐÁP ỨNG KHÁNG THỂ SAU KHI TIÊM 2 LIỀU VACINE SARS-CoV-2 mRNA TRÊN NỀN BỆNH NHÂN GHÉP TẠNG
Brian J. Boyarsky, MD, PhD1; William A. Werbel, MD2; Robin K. Avery, MD2; et alAaron A. R. Tobian, MD, PhD3; Allan B. Massie, PhD1; Dorry L. Segev, MD, PhD1; Jacqueline M. Garonzik-Wang, MD, PhD1
Nguồn: JAMA. Published online May 5, 2021. doi:10.1001/jama.2021.7489
Giới thiệu
Khác với khả năng đáp ứng miễn dịch của những người tham gia nghiên cứu thử nghiệm, khoảng chừng 17% những người ghép tạng (solid organ transplant recipients) có kháng thể sau khi tiêm liều đầu vaccine SARS-CoV-2 messenger RNA (mRNA). Những người đang điều trị thuốc chống thải ghép, ức chế miễn dịch (anti–metabolite maintenance immunosuppression) có tỉ lệ đáp ứng thấp hơn. Nghiên cứu này nhằm mục đích đánh giá đáp ứng kháng thể sau khi tiêm liều 2 vacine SARS-CoV-2 messenger RNA (mRNA).
Phương pháp nghiên cứu
Những người được ghép tạng trên toàn nước Mỹ chưa nhiễm Covid 19 trước đó (PCR–Confirmed COVID-19) được lựa chọn để tham gia nghiên cứu thông qua chiến dịch quảng bá kỹ thuật số (digital campaign). Những người tham gia được tiêm 2 vaccine SARS-CoV-2 mRNA từ ngày 16 tháng 12 năm 2020 đến ngày 13 tháng 3 năm 2021; và được theo dõi chặt chẽ cho đến ngày 13 tháng 4 năm 2021.Như đã mô tả trước đây, xét nghiệm bán định lượng kháng protein đột biến trong huyết thanh (Semiquantitative Antispike Serologic) đã được thực hiện bằng phương pháp phân tích miễn dịch Roch kháng enzyme SARS-CoV-2S (Roche Elecsys anti–immunoassay). Ngưỡng dương tính tối thiểu phải đạt 0.8U/mL đối với những test nhận diện phạm vi kết hợp thụ thể protein đột biến SARS-CoV-2 (the receptor-binding domain of the SARS-CoV-2 spike protein). Hoặc phương pháp phân tích enzyme miễn dịch EUROIMMUN (EUROIMMUN enzyme immunoassay), ngưỡng dương tính tham chiếu bất kỳ phải đạt tối thiểu 1.1 đơn vị nhiệm ý (Arbitrary Units-AU). Đây là 2 phương pháp phổ biến xác định đáp ứng miễn dịch trên người hiện nay. Công trình nghiên cứu này được bộ phận thẩm định và phê duyệt nghiên cứu Đại học Johns Hopkins chấp thuận. Thỏa thuận Tham Gia Nghiên Cứu (Informed Consent) đạt được bằng phiên bản điện tử từ các đối tượng tham gia.
Tỉ lệ bệnh nhân có kháng thể đáp ứng dương tính được đánh giá với khoản tin cậy chính xác. Fisher test được sử dụng để so sánh những biến cố định như chống thải ghép, ức chế miễn dịch và Kruskal-Wallis Test sử dụng để phân tích các biến liên diễn(Continuos Variables). Tất cả các test là 2 sided test với α = .05. Phần mềm Stata 16.1/Windows được sử dụng để phân tích số liêu.
Kết quả
Tổng cộng 658 người ghép tạng được tiêm 2 liều vaccine SARS-CoV-2 mRNA. Có 396 người đã tiêm liều 1 trước đó và kết quả tiêm liều đầu đã được khai báo. Trung bình 21 ngày sau khi tiêm liều thứ nhất -median 21(18-25)-kháng thể được phát hiện trên 98 người (15%) tham gia (95% CI, 12%-18%). Bình quân 29 ngày sau khi tiêm liều thứ hai – mean 29 (28-31) - kháng thể được phát hiện trên 357 người chiếm 54% số người tham gia (95% CI, 50%-58%). (Bản 1)
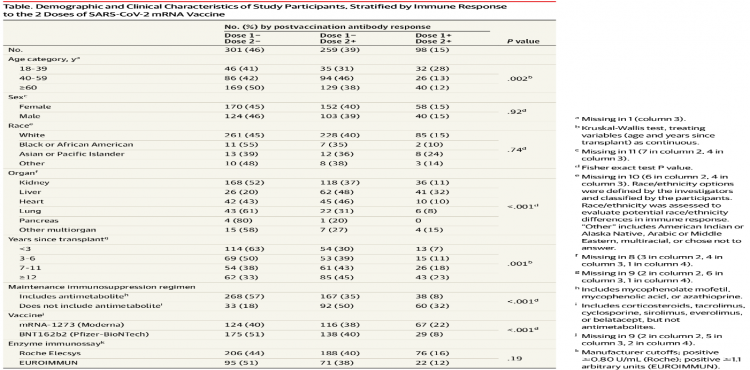
Trong tổng số 658 đối tượng tham gia nghiên cứu, có 98 người (15%) đo được lượng kháng thể đáp ứng sau khi tiêm liều 1 và 2. Có 301người (46%) không có kháng thể khi sau khi tiêm liều 1 hoặc 2. Và có 2599 người (39%) không có kháng thể sau khi tiêm liều 1 nhưng sinh ra kháng thể sau khi tiêm liều 2.
Trong tổng số 658 người tham gia nghiên cứu, kháng thể bình quân sau khi tiêm vaccine liều 2 là 14 U/mL (0.4-245.8) (Roche) và 1.239 AU (0.13-6.38) khi dùng test EUROIMMUN). Trong số 357 trường hợp phát hiện kháng thể sau khi tiêm liều 2, mức độ kháng thể trung bình là 142.1 U/mL (9.44-250) khi sử dụng Roche test và 6.48 AU (3.75-8.72) khi sử dụng EUROIMMUN test. 34.7 U/mL (5.38->250) (Roche) and 5.05 AU (2.33-7.02) (EUROIMMUN) trong số 259 người không có kháng thể đáp ứng sau khi tiêm liều 1; và nhiều hơn 250 U/mL (250-250) (Roche) và 9.23 AU (8.62-9.73) (EUROIMMUN) trong số 98 người có kháng thể sau khi tiêm liều 1.
Trong số 473 người đang sử dụng thuốc chống chuyển hóa (antimetabolites), 38 người (8%) phát hiện có kháng thể sau khi tiêm liều 1 và 2. 268 người (57%) không tìm thấy kháng thể sau khi tiêm liều 1 và 2; và 167 người (35%) không tìm thấy kháng thể sau khi tiêm liều 1 và nhưng có kháng thể sau khi tiêm liều 2. Trong tổng số 185 người không sử dụng thuốc chống chuyển hóa, có 60 người (32%) phát hiện có kháng thể sau khi tiêm liều 1 và 2; 33 người (18%) không tìm thấy kháng thể sau khi tiêm liều 1 và 2. Và 92 người (50%) không tìm thấy kháng thể sau khi tiêm liều 1 nhưng có kháng thể khi tiêm liều 2.
Bàn luận
Trong nghiên cứu đáp ứng thể dịch đối với vaccine tiêm 2 liều mRNA SARS-CoV-2 vaccine trên nền các bệnh nhân ghép tạng, phần lớn phát hiện có kháng thể đáp ứng sau khi tiêm liều 2, mặc dù người tham gia không đáp ứng sau khi tiêm liều thứ nhất nhìn chung có kháng thể thấp. Đáp ứng thể dịch có liên quan trực tiếp đến các bệnh nhân dùng thuốc chống chuyển hóa đào thải mảnh ghép.
Mặc dù chưa xác định ngưỡng (threshold) miễn dịch bảo vệ, mức độ kháng thể là khá thấp và đã quan sát được ở các loại vaccine tạo khả năng miễn dịch
Giới hạn của nghiên cứu này bao gồm cỡ mẫu thiếu tính tổng thể và bao quát (external validity), thiếu nhóm chứng về khả năng miễn dịch thiếu đánh giá sau khi tiêm vaccine và thiếu thăm dò đáp ứng tế bào nhớ B và T (memory B-cell or T-cell responses).
Mặc dù nghiên cứu cho thấy cải thiện đáp ứng kháng thể kháng protein đột biến trên nền bệnh nhân ghép tạng sau khi tiêm liều 2 so với liều 1, số liệu cũng chỉ ra rằng những người ghép tạng vẫn có nguy cơ cao nhiễm COVID-19 sau khi tiêm đủ 2 liều mRNA vaccine. Các nghiên cứu trong tương lai nên đề cập đến các giải pháp nhằm cải thiện đáp ứng của vaccine trên nhóm bệnh nhân này, bao gồm tăng liều vaccine hoặc điều chỉnh liệu trình dùng thuốc ức chế miễn dịch (immunosuppression modulation)
Tham khảo
- Walsh EE, Frenck RW Jr, Falsey AR, et al. Safety and immunogenicity of two RNA-based Covid-19 vaccine candidates. N Engl J Med. 2020;383(25):2439-2450.doi:10.1056/NEJMoa2027906PubMedGoogle ScholarCrossref
- Jackson LA, Anderson EJ, Rouphael NG, et al; mRNA-1273 Study Group. An mRNA vaccine against SARS-CoV-2. N Engl J Med. 2020;383(20):1920-1931. doi:10.1056/NEJMoa2022483PubMedGoogle ScholarCrossref
- Boyarsky BJ, Werbel WA, Avery RK, et al. Immunogenicity of a single dose of SARS-CoV-2 messenger RNA vaccine in solid organ transplant recipients.JAMA. Published online March 15, 2021. doi:10.1001/jama.2021.4385ArticlePubMedGoogle Scholar
- Klein SL, Pekosz A, Park HS, et al. Sex, age, and hospitalization drive antibody responses in a COVID-19 convalescent plasma donor population. J Clin Invest. 2020;130(11):6141-6150. doi:10.1172/JCI142004PubMedGoogle ScholarCrossref
- Patel EU, Bloch EM, Clarke W, et al. Comparative performance of five commercially available serologic assays to detect antibodies to SARS-CoV-2 and identify individuals with high neutralizing titers. J Clin Microbiol. Published online January 21, 2021. doi:10.1128/JCM.02257-20PubMedGoogle Scholar.
- Mueller T. Antibodies against severe acute respiratory syndrome coronavirus type 2 (SARS-CoV-2) in individuals with and without COVID-19 vaccination: a method comparison of two different commercially available serological assays from the same manufacturer. Clin Chim Acta. 2021;518:9-16. doi:10.1016/j.cca.2021.03.007PubMedGoogle ScholarCrossref
Người dịch: Bác sỹ Hồ Ngọc Kính
Đại học Phan Châu Trinh
Các tin khác
- Liệu pháp Hormone Nữ hóa (fGAHT): Hướng dẫn Chăm sóc Y tế Toàn diện ( 14:09 - 28/07/2025 )
- Phẫu thuật Mitrofanoff: 40 năm nhìn lại ( 13:19 - 26/06/2025 )
- SỰ KHÁC BIỆT ĐÁP ỨNG MIỄN DỊCH GIỮA CÁC VACCINE COVID-19 VÀ THỜI GIAN BÁN HỦY KHÁNG THỂ KHÁNG GAI SARS-COV-19 ( 14:16 - 29/05/2023 )
- Ket quả xác đinh omicron của 40 mau PCTU thực hiện ( 15:51 - 21/02/2022 )
- Nghiên cứu: Thuốc kháng viêm có thể gây ra phản ứng miễn dịch yếu hơn với vắc-xin Covid-19 ( 10:09 - 11/06/2021 )
- Kháng thể đặc hiệu SARS-CoV-2 trong sữa mẹ sau khi phụ nữ cho con bú được chủng ngừa COVID-19 ( 10:48 - 31/05/2021 )
- Hiệu quả của điều trị kháng sinh làm giảm nguy cơ tử vong hoặc giảm tỉ lệ bệnh đường hô hấp mắc phải tại bệnh viện ở những người cao tuổi bị bệnh xơ hóa phổi chưa rõ nguyên nhân ( 08:43 - 14/05/2021 )
- NHIỆT ĐỘ MIỆNG Ở BỆNH NHÂN NHẬP VIỆN KHÔNG BỊ NHIỄM TRÙNG ( 08:08 - 13/05/2021 )
- Ung thư - Điều trị nhắm đích và các xét nghiệm dẫn đường ( 10:42 - 08/09/2020 )
- Tỷ lệ và sự phân bố các typ Papilloma vi rút ( 10:36 - 08/09/2020 )